- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Равновесные кривые в координатах x-y и T-x-y
При заданных давлении и температуре состав пара над жидкостью является строго определенным и зависит только от состава жидкости. В этом случае пар и азот находятся в равновесном состоянии. Если нарушить это равновесие, то изменится состав жидкой и паровой фаз. Для определения зависимости между равновесными содержаниями компонентов смеси в жидкости и паре пользуются графиком (рис. 2.2). По оси абсцисс откладывают концентрацию компонентов в жидкости x, а по оси ординат – концентрацию этого же компонента в паре у.
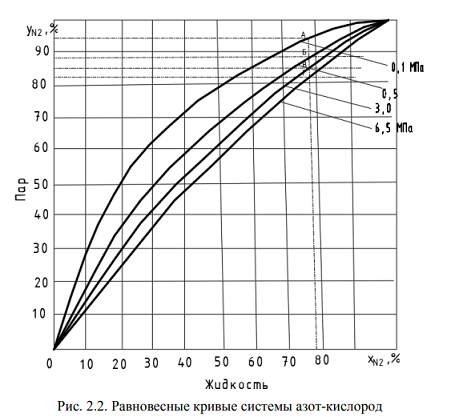
Например, если концентрация азота в жидкости 78% (см. рис. 2.2) при давлении 0,1 МПа, то в паре над жидкостью его будет содержаться 93% (точка А). С увеличением давления содержание низкокипящего компонента (азота) в паре уменьшается, а высококипящего (кислорода) увеличивается. При давлении 0,5 МПа концентрация азота в паре 90% (точка Б), при давлении 3 МПа – 85% (точка В).
При повышении давления кислородно-азотной смеси концентрация N2 и О2 в паре стремится к концентрации их в жидкости. Если нарушить равновесие системы, отбирая пар над жидкостью, то жидкость будет обогащаться кислородом, а азот, как наиболее летучий компонент, станет переходить в пар. Температура жидкой фазы повысится; эта температура будет тем выше, чем больше давление жидкости.
Отложим по оси абсцисс концентрацию азота в жидкости, а по оси ординат температуру кипения жидкости при постоянном давлении (рис. 2.3).
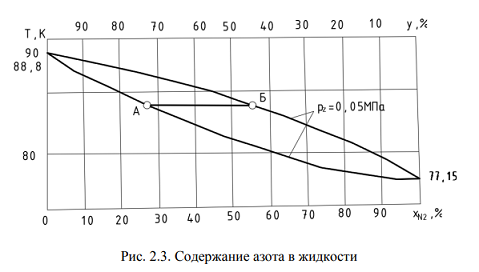
Кривые показывают, как меняется концентрация жидкости в зависимости от температуры (нижняя кривая) и как изменяется состав пара над кипящей жидкостью – (верхняя кривая). С понижением температуры при p-const концентрация азота в жидкости повышается и приближается к 100%, с повышением температуры жидкости концентрация азота в жидкости уменьшается.
Эта разность наибольшая, когда в жидкости содержится 30…40% N2. С увеличение давления жидкости разность содержания азота в жидкой и паровой фазах (отрезок АБ) уменьшается, а при критическом давлении она равна нулю (рис. 2.4).
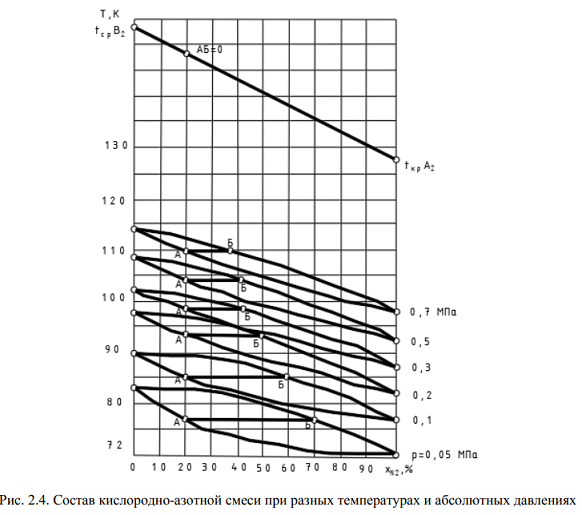
Следовательно, процесс разделения (ректификации) выгоднее проводить при более низком давлении, так как при этом разность (отрезок АБ) между жидкой и паровой фазами будет больше.
Статьи по теме
- Определение поверхности нагрева или продолжительности процесса выпаривания для выпарных аппаратов периодического действия
- Выпаривание с минимальной общей поверхностью нагрева
- Выпаривание при одинаковых поверхностях нагрева всех корпусов
- Распределение полезной разности температур по корпусам выпарной установки
- Определение полной температурной депрессии в выпарной установке
- Материальный баланс процесса выпаривания
- Схемы многокорпусных установок
- Принцип многократного испарения
- Классификация выпарных аппаратов
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

